Crossject franchit une nouvelle étape clé dans la fabrication de ZEPIZURE®
18 Julio 2024 - 12:30AM
UK Regulatory
Crossject franchit une nouvelle étape clé dans la fabrication de
ZEPIZURE®
- Fabrication réussie d’un autre Lot
Règlementaire de ZEPIZURE® sur le nouveau site de fabrication
- Une étape importante qui complète
les résultats satisfaisants obtenus avec les lots précédents dans
le cadre des études de stabilité, et qui s'inscrit dans la
continuité des données de fabrication positives générées depuis
2021
- Une étape dans la fabrication qui
contribuera au succès de la procédure d’urgence (EUA) de la FDA
conformément au plan de marche
Dijon, France, le 18 juillet 2024, 07:30
CET -- Crossject (ISIN: FR0011716265; Euronext: ALCJ), société
pharmaceutique de spécialités en phase avancée de développement
réglementaire de ZEPIZURE®, traitement d’urgence dans la prise en
charge des crises d’épilepsie basé sur l’auto-injecteur sans
aiguille primé ZENEO®, annonce l'achèvement avec succès
d'un nouveau lot règlementaire de ZEPIZURE® dans les installations
qualifiées d'Eurofins. Eurofins est désigné comme le partenaire
CDMO qui assurera les activités de remplissage et l’assemblage
final pour les livraisons à la Biomedical Advanced Research and
Development Authority (BARDA*) des États-Unis.
Cette étape fait suite à un lot précédent
produit sur le même équipement de remplissage en décembre 2023, qui
avait donné de bons résultats et fait partie du programme de
fabrication de divers lots sur le site commercial, visant à
confirmer notamment la durée de péremption de ZEPIZURE®. Ces
nouvelles avancées sont en ligne avec les précédentes données de
stabilité à long terme.
Les lots de fabrication sont des éléments
essentiels du dossier qui sera soumis à la FDA en relation avec la
demande d’autorisation de ZEPIZURE® dans le cadre de sa procédure
d’urgence (EUA). Combinés à notre prochaine étude de bioéquivalence
aux États-Unis, ils constitueront aussi une pièce centrale de nos
futurs dossiers de demande d'autorisation de mise sur le marché
(NDA) à partir de 2025.
L'achèvement de ce lot d'enregistrement ouvre
maintenant la voie à la collecte de nouvelles données qui
démontreront davantage la qualité des produits fabriqués avec le
nouvel équipement et assureront son adéquation réglementaire à une
large utilisation commerciale, débutant avec sa livraison au
Strategic National Stockpile américain. Crossject anticipe ses
prochaines étapes avec la FDA concernant l'autorisation selon la
procédure d’urgence (EUA) de ZEPIZURE® dans l’état de mal
épileptique pour le T1 2025.
Patrick Alexandre, CEO of
Crossject a déclaré « Nous sommes très satisfaits
des progrès réalisés dans la mise en place d'un nouveau partenaire
CDMO, augmentant nos capacités de remplissage et d’assemblage final
pour ZENEO®. La production réussie de ce nouveau lot réglementaire,
ainsi que des lots précédents, témoigne du travail acharné et du
dévouement des deux équipes au cours des 18 derniers mois. Au-delà
de ZEPIZURE®, ces succès dans notre processus de fabrication, notre
dossier réglementaire et l’expansion de nos capacités industrielles
ont une vraie valeur stratégique pour Crossject. Ils constituent
une première étape concluante dans le plus large déploiement de
notre technologie ZENEO® dans l'épilepsie et dans les autres
indications de notre pipeline.”
À propos de Crossject
Crossject SA (Euronext : ALCJ ;
www.crossject.com) est une société pharmaceutique spécialisée
émergente. Elle est en phase de développement réglementaire avancé
pour ZEPIZURE®, un traitement d’urgence dans la prise en charge des
crises épileptiques pour lequel Crossject a remporté́ un contrat*
de 60 millions de dollars auprès de l’Autorité américaine pour la
R&D avancée dans le domaine biomédical (la BARDA). ZEPIZURE®
est basé sur l’auto-injecteur sans-aiguille primé ZENEO®, qui
permet aux patients et leurs aidants non formés de réaliser
facilement et instantanément une injection intramusculaire en
situation d’urgence, sur peau nue ou même à travers les vêtements.
La société développe actuellement d’autres produits, notamment pour
le traitement d'urgence des chocs allergiques, des insuffisances
surrénales, des overdoses d’opioïdes et des crises d’asthme.
* No de contrat : 75A50122C00031 avec le
Department of Health and Human Services; Administration for
Strategic Preparedness and Response; Biomedical Research and
Development Authority
Pour plus d’informations, merci de
contacter:
Investisseurs
Natasha Drapeau
Cohesion Bureau
+41 76 823 75 27
natasha.drapeau@cohesionbureau.com
|
Media
Sophie Baumont
Cohesion Bureau
+33 6 27 74 74 49
sophie.baumont@cohesionbureau.com |
|


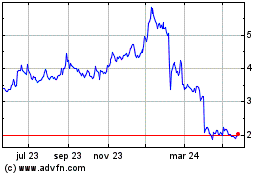
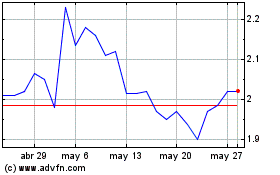
Crossject (EU:ALCJ)
Gráfica de Acción Histórica
De Sep 2024 a Oct 2024
Crossject (EU:ALCJ)
Gráfica de Acción Histórica
De Oct 2023 a Oct 2024